Linfociti: cosa dovresti sapere!
definizione
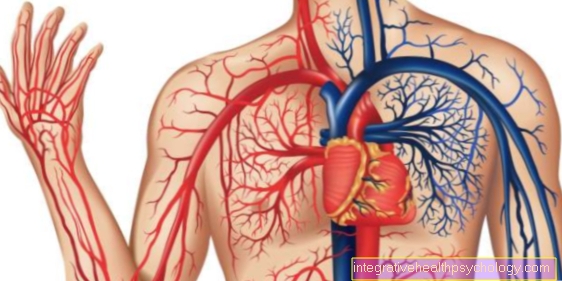
I linfociti sono un sottogruppo altamente specializzato di leucociti, i globuli bianchi che appartengono al sistema immunitario, il sistema di difesa dell'organismo. Il loro nome deriva dal sistema linfatico, poiché sono particolarmente comuni lì.
Il suo compito principale è principalmente quello di difendere l'organismo da agenti patogeni come Virus o batteri. A tale scopo, alcune cellule sono specializzate in un solo agente patogeno, motivo per cui si parla di sistema immunitario specifico o adattativo.
Ma aiutano anche ad eliminare le cellule del corpo mutate, le cosiddette cellule tumorali, che possono portare al cancro. Si distingue tra linfociti B e T e cellule natural killer, ciascuno con funzioni diverse.

Funzione dei linfociti
Se un agente patogeno entra nel corpo, viene prima attivato da cellule di difesa non specifiche, ad es. Macrofagi ("cellule giganti che mangiano") assorbiti e scomposti. I macrofagi a loro volta mostrano frammenti del patogeno, i cosiddetti antigeni, sulla loro superficie e quindi attivano le cellule T-helper, che fungono da mediatori tra le diverse cellule immunitarie specifiche, i linfociti. I linfociti assicurano che il sistema immunitario sia molto adattabile e possa reagire a varie minacce in modo finemente regolato.
La seguente reazione è suddivisa in risposta immunitaria umorale e cellulare:
La risposta immunitaria umorale (= i fluidi corporei) si basa sugli anticorpi, una certa forma di proteine, che vengono prodotti e rilasciati dalle plasmacellule. È progettato principalmente per agenti patogeni che possono moltiplicarsi indipendentemente, ad es. Batteri, ma anche altri organismi unicellulari. Gli anticorpi possono, ad esempio, aderire alla superficie dei batteri e aggregarli (agglutinazione) grazie alla loro forma speciale. Questo a sua volta rende più facile per le cellule immunitarie aspecifiche trovare l'agente patogeno ed eliminarlo. Gli anticorpi possono anche svolgere una serie di altre funzioni (vedere Linfociti B).
La risposta immunitaria cellulare è focalizzata principalmente sui virus, ma anche su alcuni batteri, che non possono vivere in modo indipendente e devono quindi attaccare le cellule del corpo. Se una cellula viene attaccata, può mostrare frammenti del parassita su speciali recettori sulla sua superficie. Le cellule T killer distruggono le cellule infette e quindi impediscono l'ulteriore diffusione dell'agente patogeno.
Maggiori informazioni su questo argomento: sistema immunitario ad esempio Linfociti T.
Anatomia e sviluppo dei linfociti
I linfociti sono di dimensioni molto variabili con 6-12 µm e sono particolarmente evidenti a causa del grande nucleo scuro che riempie quasi l'intera cellula. Il resto della cellula può essere visto come un sottile confine citoplasmatico in cui sono presenti solo pochi mitocondri per la produzione di energia e ribosomi per la produzione di proteine.
Si presume che le forme più grandi di linfociti, che hanno anche un nucleo cellulare più leggero (= eucromatico), siano state attivate da un attacco batterico o virale. I linfociti inattivi più piccoli, chiamati anche ingenui, sono molto più comuni nelle persone sane e hanno all'incirca le stesse dimensioni dei globuli rossi (eritrociti).
Maggiori informazioni su: Eritrociti
I linfociti derivano dallo stadio intermedio dei linfoblasti dalle cellule staminali ematopoietiche (ematopoiesi = formazione del sangue), che negli adulti si trovano principalmente nel midollo osseo.Qui le cellule precursori (progenitori) dei linfociti differiscono da quelle delle altre cellule (mieloidi) in quanto alcune di esse continuano a maturare nel timo (chiamate anche animelle). Questi sono successivamente chiamati linfociti T ("T" per il timo). La maturazione nel timo persegue lo scopo di smistare tutti quei linfociti T che reagiscono alle strutture proprie del corpo o sono comunque limitati nella loro funzione (selezione positiva e negativa).
Per ulteriori informazioni, vedere: Linfociti T.
I linfociti B e le cellule NK (cellule natural killer), invece, completano la loro maturazione come gli altri globuli del midollo osseo (“B” per “midollo osseo” o storicamente Bursa fabricii, organo degli uccelli). Dopo che i linfociti B hanno lasciato il midollo osseo come cellule mature, ingenue (= non specializzate), entrano in organi come milza, tonsille o linfonodi, dove possono entrare in contatto con antigeni (strutture estranee). A tale scopo, la cellula trasporta alcuni anticorpi sulla sua superficie, che fungono da recettori delle cellule B. Le cosiddette cellule dendritiche, un altro tipo di cellula immunitaria che non appartiene ai linfociti, presentano frammenti di antigene ai linfociti B ingenui e li attivano con l'aiuto delle cellule T helper. Se una cellula B è stata attivata, si divide più volte e si trasforma in una plasmacellula (selezione clonale).
I diversi tipi di linfociti sembrano molto simili, ma possono essere differenziati l'uno dall'altro utilizzando speciali metodi di marcatura e colorazione (immunoistochimica) al microscopio.
Linfociti B.
Quando viene attivato, la maggior parte delle cellule B mature si sviluppa in plasmacellule, il cui compito è generare anticorpi contro sostanze estranee. Gli anticorpi sono proteine a forma di Y che possono legarsi a strutture molto specifiche, i cosiddetti antigeni. Si tratta principalmente di proteine, ma spesso anche di zuccheri (carboidrati) o lipidi (molecole contenenti grassi). Gli anticorpi sono anche chiamati immunoglobuline e sono suddivisi in 5 classi in base alla struttura e alla funzione (IgG, IgM, IgD, IgA e IgE).
Gli anticorpi ora aiutano in vari modi a combattere l'infezione: ad esempio, i veleni come la tossina del tetano possono essere neutralizzati o l'intero agente patogeno può essere marcato. Un patogeno marcato in questo modo può ora da un lato essere assorbito e digerito da alcune cellule immunitarie, i macrofagi e i granulociti neutrofili. L'agente patogeno può, tuttavia, essere distrutto e sciolto anche da cellule natural killer, nonché da macrofagi e granulociti da sostanze tossiche per l'agente patogeno. Alcuni anticorpi possono anche raggruppare le cellule bersaglio per renderle più facili da rilevare e per renderle più ricettive.
Un altro modo è tramite l'attivazione del sistema del complemento, che è composto da diverse proteine aspecifiche che dissolvono le cellule marcate in una sorta di reazione a catena. Tuttavia, queste proteine sono permanentemente presenti in concentrazioni comparabili nel sangue e fanno parte del sistema immunitario innato. Inoltre, i mastociti vengono attivati da anticorpi che contengono sostanze infiammatorie come ad es. Rilascia le istamine, che aumentano il flusso sanguigno al tessuto interessato e quindi rendono più facile per altre cellule immunitarie raggiungere il centro dell'infiammazione.
potresti essere interessato anche a: istamina
Un altro sottogruppo di linfociti B si sviluppa in cellule di memoria B quando attivate, che possono sopravvivere per diversi anni. Se il corpo viene nuovamente esposto allo stesso patogeno durante questo periodo, queste cellule possono svilupparsi in plasmacellule molto più velocemente per impedire che l'infezione si diffonda in modo più efficiente. Questo crea una protezione vaccinale che dura a lungo e può durare per anni.
Per informazioni dettagliate, vedere anche: Cosa sono i linfociti B?
Linfociti T.
Esistono due gruppi principali di linfociti T, cellule T helper e cellule T killer, nonché cellule T regolatorie e, a loro volta, cellule T della memoria a lunga vita.
Le cellule T helper rafforzano l'effetto delle altre cellule immunitarie legandosi agli antigeni che si presentano su altre cellule immunitarie e quindi rilasciano citochine, una sorta di attrattivo e attivatore per altre cellule immunitarie. A seconda del tipo di cellule di difesa richieste, esistono ulteriori sottogruppi specializzati. Svolgono un ruolo speciale nell'attivazione delle plasmacellule e delle cellule T killer.
Le cellule T killer sono anche chiamate linfociti T citotossici perché, a differenza della maggior parte delle cellule immunitarie, distruggono le proprie cellule invece di quelle che sono estranee al corpo. Ciò è sempre necessario quando una cellula del corpo viene attaccata da un virus o da un altro parassita cellulare o quando una cellula viene modificata in modo tale da poter diventare una cellula cancerosa. La cellula T killer può attaccarsi a determinati frammenti di antigene che la cellula infetta trasporta sulla sua superficie e ucciderli attraverso vari meccanismi. Un esempio particolarmente noto è l'introduzione di una proteina dei pori, la perforina, nella membrana cellulare. Questo fa sì che l'acqua fluisca nella cella bersaglio, facendola scoppiare. Puoi anche far sì che la cellula infetta si autodistrugga in modo controllato.
Le cellule T regolatorie hanno una funzione inibitoria sulle altre cellule immunitarie e quindi assicurano che la reazione immunitaria non continui a svilupparsi e possa ridursi rapidamente di nuovo. Svolgono anche un ruolo importante durante la gravidanza, poiché assicurano che le cellule del feto, che alla fine sono anche estranee, non vengano attaccate.
Le cellule T della memoria, come le cellule B della memoria, si conservano a lungo e garantiscono anche una risposta immunitaria più rapida se il patogeno si ripresenta.
Cellule natural killer
Le cellule natural killer o cellule NK svolgono un ruolo simile alle cellule T killer, ma a differenza degli altri linfociti, non appartengono al sistema immunitario adattativo ma innato. Ciò significa che sono permanentemente funzionanti senza dover essere attivati in anticipo. Tuttavia, la loro risposta è difficile da regolamentare. Tuttavia, appartengono al gruppo dei linfociti perché derivano dalle stesse cellule precursori.
Maggiori informazioni sull'argomento.
- sistema immunitario
- Come puoi rafforzare il sistema immunitario?
Valori normali dei linfociti
La concentrazione di linfociti oscilla durante il giorno e dipende dall'ora del giorno, dallo stress, dallo sforzo fisico e da altri fattori. Si parla di aumento patologico solo se i linfociti sono al di sopra dei valori limite.
Per determinare il numero di linfociti, è necessario un emocromo differenziale, che fa parte dell'emocromo di grandi dimensioni. La proporzione di linfociti nella conta leucocitaria totale (leucociti = globuli bianchi) dovrebbe essere compresa tra il 25 e il 40%, che corrisponde a una concentrazione di 1.500-5.000 / µl. Se il valore è superiore a questo si parla di linfocitosi, se è inferiore si parla di linfocitopenia (detta anche linfopenia). Nei bambini piccoli la concentrazione di leucociti può essere notevolmente più alta e la proporzione di linfociti può arrivare fino al 50%.
Maggiori informazioni su: Emocromo
Quale può essere la causa se i linfociti sono aumentati?
Infezioni come causa di un aumento dei linfociti
Nella maggior parte dei casi, un aumento del numero di linfociti (= linfocitosi) indica un'infezione da virus, poiché i linfociti sono particolarmente adatti per combatterli. Fondamentalmente, con tutte le infezioni da virus, ci si può aspettare almeno una concentrazione di linfociti leggermente aumentata.
Inoltre, alcune infezioni batteriche come pertosse (pertosse, tosse secca), tubercolosi (consumo), sifilide, tifo (febbre enterica, febbre parentale) o brucellosi (febbre mediterranea, febbre di Malta) innescano un caratteristico aumento dei linfociti. Il numero di linfociti rimane aumentato anche con decorsi cronici, cioè di lunga durata. Altri parassiti come Toxoplasma gondii possono anche portare ad un aumento a breve termine dei linfociti.
Maggiori informazioni su: Malattie infettive
Malattie autoimmuni
Tuttavia, ci sono anche malattie infiammatorie senza infezione che portano ad un aumento del numero di linfociti, come B. le malattie intestinali Morbus Crohn e la colite ulcerosa, nonché malattie autoimmuni come Morbus Graves, in cui i linfociti formano anticorpi contro le cellule tiroidee, per cui queste sono eccessivamente eccitate, il che a sua volta disturba l'equilibrio ormonale. Anche il sarcoide (morbo di Boeck), un particolare tipo di infiammazione che colpisce particolarmente i polmoni, può portare ad un aumento del numero di linfociti.
Ulteriori informazioni possono essere trovate qui: sarcoide
Malattia della tiroide
Tuttavia, un equilibrio disturbato degli ormoni tiroidei, come nel caso di una tiroide iperattiva (ipertiroidismo) o del morbo di Addison (insufficienza surrenalica primaria), può anche portare a un aumento della conta linfocitaria.
potresti essere interessato anche a: morbo di Addison
Aumento dei leucociti a causa di malattie tumorali
Una linfocitosi particolarmente grave può svilupparsi in alcune neoplasie, cioè cellule tumorali maligne:
Nella leucemia linfocitica cronica (LLA), sono le cellule precursori dei linfociti che si sono sviluppate in cellule tumorali a causa delle mutazioni. È la forma più comune di leucemia nel mondo occidentale. Poiché si verifica particolarmente frequentemente intorno ai 50 anni, viene anche chiamata "leucemia dell'età".
La leucemia linfoblastica acuta deriva anche da cellule precursori dei linfociti, ma di solito è accompagnata da una rapida degenerazione del midollo osseo, che può portare all'anemia, poiché le altre cellule del sangue non possono svilupparsi adeguatamente. Di conseguenza, in alcuni casi non è possibile determinare alcun cambiamento o addirittura una diminuzione dei leucociti totali. Il numero anormalmente aumentato di linfociti è evidente solo nella conta ematica differenziale.
Poiché i linfociti mutati sono generalmente privi di funzione in entrambe le malattie, si può presumere una riduzione delle prestazioni del sistema immunitario nonostante l'aumento del numero.
Inoltre, altri tumori maligni che colpiscono altre cellule del sistema linfatico possono scatenare la linfocitosi, ad esempio il linfoma di Hodgkin (malattia di Hodgkin, linfogranulomatosi, linfogranuloma), ma anche alcuni linfomi non Hodgkin.
Leggi anche: Linfoma di Hodgkin ad esempio leucemia
Quale può essere la causa se i linfociti sono bassi?
La linfocitopenia si verifica spesso a seguito della terapia e in questo contesto non è considerata patologica: ciò è particolarmente comune quando si trattano corticoidi, in particolare cortisone, e quando si somministrano globuline antilinfocitarie. Entrambi sono usati specificamente per sopprimere le reazioni infiammatorie. Ulteriori forme di terapia che possono causare una carenza di linfociti sono le radiazioni e la chemioterapia, entrambe utilizzate per la terapia del cancro, ma possono anche influenzare le cellule del corpo in rapida divisione come i precursori delle cellule del sangue. Inoltre, questo fenomeno è stato osservato quando è stato somministrato il farmaco ganciclovir, che viene utilizzato principalmente per trattare il citomegalovirus (CMV, herpesvirus umano 5, HH5). Durante il trattamento con luce UV a onde lunghe (UVA), spesso viene somministrata anche la sostanza naturale psoralene per il suo effetto fotosensibilizzante, che può anche avere un effetto riducente sulla conta leucocitaria.
Un altro possibile motivo della linfocitopenia è la malnutrizione a basso contenuto proteico o lo stress costante, che può aumentare in modo permanente il livello di cortisolo (vedi terapia con cortisone). Esistono anche quadri clinici con cause organiche come la malattia di Cushing, che stimola il midollo surrenale a produrre un aumento del cortisolo a causa di un malfunzionamento della ghiandola pituitaria (adenoipofisi). Anche alcune malattie autoimmuni come l'artrite reumatoide, il lupus eritematoso sistemico (lichene della farfalla) e l'enteropatia essudativa (gastro) (sindrome di Gordon) possono portare a linfopenia.
Nell'uremia, a causa di una disfunzione renale, si accumulano nel sangue sostanze che, nelle persone sane, vengono scaricate attraverso l'urina. Oltre a una serie di altri sintomi, questo porta anche a una diminuzione della funzione dei leucociti.
Poiché un'infezione con il virus HI (virus dell'immunodeficienza umana, innesca l'AIDS) colpisce e distrugge in particolare le cellule T helper, anche in questo caso ci si può aspettare un forte calo del numero di linfociti.
Esistono anche cause congenite che influenzano maggiormente lo sviluppo dei linfociti (linfocitopoiesi) e sono innescate da mutazioni nei geni di alcuni enzimi. Questi includono il deficit di adenosina deaminasi e il deficit di fosforilasi nucleosidica purinica, nonché la sindrome di Wiskott-Aldrich, che colpisce principalmente i trombociti (piastrine del sangue) a causa della formazione disturbata del sistema citoscheletrico; la linfocitopenia e l'immunodeficienza di solito si sviluppano solo negli anni successivi della vita.
Inoltre, alcuni linfomi di Hodgkin (malattia di Hodgkin, linfogranulomatosi, linfogranuloma) e singoli linfomi non Hodgkin, ovvero il cancro dell'intero sistema linfatico, possono compromettere lo sviluppo dei linfociti e di conseguenza ridurne il numero.
Leggi anche: Myastenia gravis o HIV
Come cambiano i linfociti con il raffreddore?
I termini comuni raffreddore e infezione simil-influenzale indicano una serie di diverse e lievi malattie delle vie respiratorie, che sono principalmente causate da virus, ma occasionalmente anche da batteri.
È tipico delle infezioni batteriche che il numero totale di leucociti aumenti (= leucocitosi), che di solito colpisce anche i linfociti. Nelle infezioni virali, il numero totale di leucociti tende ad essere inferiore (= leucopenia), il che è spesso dovuto al fatto che il sistema immunitario non riesce a tenere il passo con la produzione di cellule di difesa, ma alcuni virus possono anche inibire direttamente il sistema immunitario. È caratteristico, tuttavia, che il numero dei linfociti rimanga stabile o addirittura aumenti, poiché questi sono particolarmente indicati per combattere le infezioni virali e quindi si sviluppano preferenzialmente dalle comuni cellule staminali.
Come cambiano i linfociti nell'HIV?
Il virus HI (virus dell'immunodeficienza umana) attacca le cellule che hanno una specifica proteina di superficie, il CD4 (cluster di differenziazione). Si tratta principalmente di cellule T helper, che vengono distrutte dalla replicazione del virus, che riduce drasticamente il numero di linfociti (linfopenia). La perdita di cellule T helper funzionali supera il numero di cellule infette, per cui devono svolgere un ruolo anche i meccanismi di inibizione indiretta, che ad esempio influiscono sulla maturazione dei linfociti. Inoltre, vengono attaccati anche i macrofagi (fagociti giganti), sebbene questi non contino tra i linfociti e solo una percentuale relativamente piccola muore.
Nella primissima fase, circa 1-4 settimane dopo l'infezione (infezione primaria), i pazienti spesso mostrano sintomi simili al raffreddore per circa una settimana. Tuttavia, qui la conta leucocitaria di solito aumenta leggermente mentre il numero di linfociti diminuisce. Questo è spesso seguito da un periodo senza sintomi in cui il numero di linfociti diminuisce solo molto lentamente, rimane stabile o addirittura si normalizza. Questa condizione può durare per diversi anni e spesso passa inosservata fino a quando, se non trattata, alla fine si trasforma in AIDS.
Ulteriori informazioni sull'HIV possono essere trovate Qui.
Durata della vita dei linfociti
La durata della vita dei linfociti può essere molto diversa a causa dei diversi compiti: i linfociti che non vengono mai a contatto con gli antigeni (strutture di corpo estraneo) muoiono dopo pochi giorni, mentre i linfociti attivati ad es. Le plasmacellule possono sopravvivere per circa 4 settimane. Le cellule della memoria sopravvivono più a lungo, poiché possono sopravvivere per diversi anni e quindi contribuire alla memoria immunologica.
Secondo scoperte più recenti, ci sono anche plasmacellule a lunga vita che continuano a produrre anticorpi appropriati anche dopo che l'infezione si è attenuata e quindi garantiscono un titolo anticorpale stabile (= livello di diluizione).
L'immunità permanente si ottiene solitamente solo con vaccini vivi, per cui ci si può aspettare che una porzione estremamente piccola e innocua del vaccino rimanga nell'organismo.
Cos'è il test di trasformazione dei linfociti?
Il test di trasformazione dei linfociti (LTT) è un metodo per la rilevazione di speciali linfociti T, ognuno dei quali si è specializzato in un determinato antigene (frammento di corpo estraneo). Recentemente è stato utilizzato principalmente nella diagnostica delle funzioni immunitarie, ma anche in allergologia per la rilevazione di allergie a determinati farmaci o metalli, che si manifestano solo dopo un certo ritardo. Attualmente è consigliato principalmente come supplemento al patch test. Questo test è un test di provocazione per verificare le allergie da contatto. Inoltre, il valore informativo viene attualmente utilizzato come test di rilevamento per alcuni agenti patogeni come Malattia di Lyme discussa in modo controverso.
Nella prima fase del test di trasformazione dei linfociti, i linfociti vengono separati dalle altre cellule del sangue mediante diversi processi di lavaggio e centrifugazione (un processo che scompone i componenti del sangue in base alla loro massa). Le cellule, insieme all'antigene in esame, vengono quindi lasciate a se stesse per alcuni giorni in condizioni di crescita ottimali. Un campione di controllo rimane senza antigene.16 ore prima della valutazione, viene aggiunta la timina marcata radioattivamente, un componente del DNA. Trascorso il tempo, viene misurata la radioattività della coltura dei linfociti e da questo viene calcolato un cosiddetto indice di stimolazione. Ciò fornisce informazioni su se e in che misura i linfociti T sono sensibili all'antigene.
Il test si avvale del fatto che le cellule T attivate, che derivano sempre più da cellule T della memoria sensibilizzate, si convertono o si trasformano in risposta all'antigene corrispondente. Di conseguenza, condividono anche, per quale scopo devono costruire il DNA e quindi incorporare sempre più la timina radioattiva.
Tipizzazione dei linfociti
La tipizzazione dei linfociti, nota anche come stato immunitario o immunofenotipizzazione, è un processo che esamina la formazione di varie proteine di superficie, solitamente i cosiddetti marcatori CD (Cluster of Differentiation). Poiché queste proteine differiscono nei diversi tipi di linfociti, è possibile creare un cosiddetto pattern di espressione delle proteine di superficie utilizzando anticorpi codificati a colori prodotti artificialmente. Da ciò si possono trarre conclusioni sulla distribuzione dei diversi tipi, ma anche sul grado di differenziazione delle cellule. Questo metodo è quindi particolarmente adatto per la classificazione della leucemia, ma viene utilizzato anche, ad esempio, per il monitoraggio delle infezioni da HIV.
potresti essere interessato anche a: Leucemia o infezione da HIV.
Linfociti nelle urine
L'aumento del numero di linfociti nelle urine è chiamato linfocituria, che si verifica particolarmente spesso nelle infezioni virali, nei linfomi e nelle reazioni di rigetto dopo il trapianto di rene senza un aumento delle altre cellule immunitarie.
Nella maggior parte dei casi, tuttavia, solo il numero di tutti i leucociti viene considerato nel contesto dello stato delle urine, per cui si considererebbe solo una causa patologica da una concentrazione superiore a 10 / µl. Tale leucocituria si verifica spesso in relazione a un'infezione delle vie urinarie, ma può anche avere altre cause come l'infiammazione della prostata, una malattia reumatica o la gravidanza. Si parla quindi di leucocituria sterile, poiché non è stato possibile trovare batteri a parte l'aumento del numero di leucociti.
Linfociti nel CSF
Il liquido cerebrospinale, cioè il fluido in cui nuota il nostro cervello, è relativamente povero di cellule, ma i linfociti T costituiscono la maggioranza. Una concentrazione di 3 / µl è normale qui. Inoltre, ci sono anche monociti isolati, i precursori dei macrofagi ("fobia gigante"). La presenza di altre cellule del sangue è già considerata patologica.
Se la barriera sangue-liquore, che controlla quali sostanze possono passare dal sangue al liquore, rimane intatta, solo questi due tipi di cellule aumentano di conseguenza. Questo è ad es. nella meningite (meningite), nella borreliosi o nella sifilide, ma anche in malattie senza infezione come la sclerosi multipla o tumori cerebrali speciali, nonché in alcune lesioni cerebrali.